Alerta Sanitaria: Probable contaminación de Helados Soft Serve On The Go
La empresa retiró el producto en EU y el producto se distribuye en México La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), a través de la Secretaría de Salud de Michoacán (SSM), informa a la población sobre la probable…
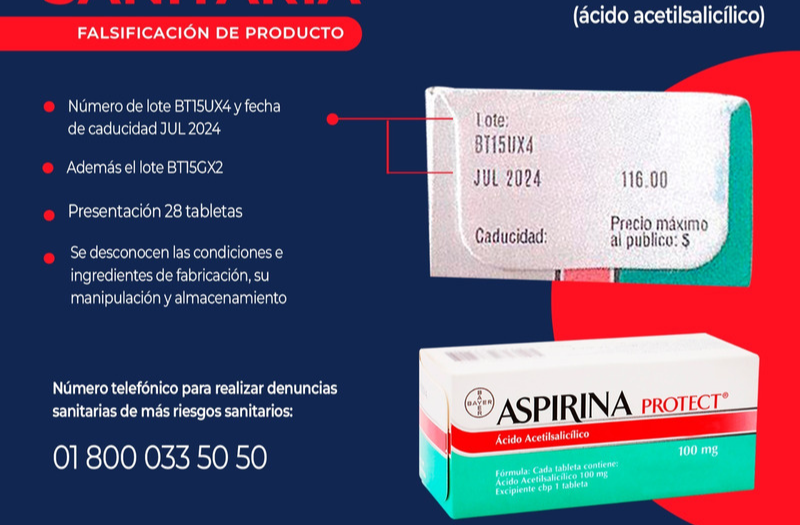
Cofepris alerta sobre Aspirina Protect falsa
El medicamento falsificado se identifica con los números de lote BT15UX4 y BT15GX2 La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) emitió alerta sanitaria a la población por la falsificación de Aspirina Protect 100 mg. Bayer…
Alerta SSM por falsificación de antídoto antialacrán
Se trata del producto Alacramyn Fragmentos F(ab ́)2, de solución inyectable. Morelia, Michoacán, 21 de julio de 2023.- La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), a través de la Secretaría de Salud de Michoacán (SSM),…
Alerta SSM por riesgos a la salud de la crema Barmicil
De manera excesiva y prolongada puede causar reacciones adversas y graves como el síndrome de Cushing. La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), a través de la Secretaría de Salud de Michoacán (SSM), alerta a la…
Alerta SSM sobre falsificación y venta de gotas oftálmicas Refresh Tears y Optive
Estos productos carecen de registro sanitario y su uso puede poner en riesgo la salud visual del consumidor. La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), a través de la Secretaría de Salud de Michoacán (SSM), alerta a la…
Cancela Cofepris venta de Redotex, medicamento “milagro” para bajar de peso; Ahora es delito comprarlo y venderlo
24 años en el mercado sólo se explican por omisiones de anteriores autoridades e influyentismo que serán investigados La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) informa que ha revocado los registros sanitarios a Redotex y…
Alerta¡ detectan venta ilegal de medicamentos para tratar Covid-19
No cuentan con registro sanitario ni con autorización en México para el tratamiento de pacientes. La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), a través de la Secretaría de Salud de Michoacán (SSM), informa a los…
¡Lo barato sale caro! Piden no comprar medicamentos en la vía pública
Además, la exposición a la intemperie puede provocar que algunas medicinas pierdan su calidad, seguridad y eficacia Cada día es más común la venta de medicamentos en la vía pública, sobre todo en mercados y tianguis, pastillas que con regularidad son…
¡Alerta para la salud! Falsifican medicamento enterogermina
Si se usó este tipo de productos y presentas algún malestar acudir con profesionales de la salud La Comisión Federal para la Protección Contra Riesgos Sanitarios (Cofepris) informa a la población sobre la falsificación y adulteración de Enterogemina® 4…
Cofepris pide a médicos no recetar el medicamento tacrolimus de la marca Octralin
La marca de este inmunosupresor cuenta con más de 50 reportes de ineficiencia terapéutica La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) instruye a profesionales de la salud no suministrar ni prescribir el medicamento…